Immune-Mediated Hemolytic Anemia (IMHA)
L’anémie hémolytique auto-immune (AHAI) est une maladie du sang qui se traduit par une baisse normale du nombre de globules rouges (aussi appelés hématies) et du taux d’hémoglobine, ce qu’on appelle une anémie. Cette maladie existe chez l’humain; chez le chien et le chat, on parle plus volontiers d’anémie hémolytique à médiation immune (AHMI).
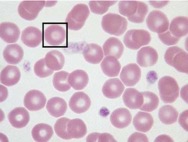
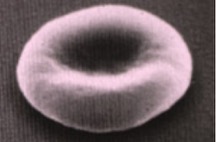
La durée de vie des globules rouges (hématies) en circulation est normalement de 120 jours; lors d’AHMI, des anticorps sont présents dans le sang. Les anticorps sont des substances fabriquées par le système immunitaire de défense de l’organisme. Ces anticorps sont des «auto-anticorps» car ils sont dirigés contre les propres globules rouges du malade; il s’agit donc «d’auto-anticorps». Les hématies sont ainsi détruites. On parle d’anémie hémolytique « auto-immune », ou à médiation immune.
La maladie peut atteindre des chiens et chats de tout âge, mais certaines prédispositions sont pourtant notées. L’AHMI est plus fréquemment rencontrée chez les chiens que chez les chats et chez les animaux d’âge moyen (dans différentes études, sont retrouvés des chiens âgés de 1 à 13 ans — médiane à six ans), un peu plus fréquemment chez les femelles.
Certaines races, comme les Cockers, les Labradors (moins les Golden Retrievers), les Bichons frisés, les Caniches, les Spitz finnois, les Rottweilers, les Bobtails, les Setters irlandais, les Pinscher nains et les Collies semblent prédisposées.
Certaines études pointent une augmentation de l’AHMI au printemps, sans déterminer les éléments favorisant cette variation saisonnière.
Il existe différents types d’AHMI:
Selon le type et les caractéristiques des auto-anticorps en cause, on distingue deux types d’AHMI :
-
-
- les AHMI à auto-anticorps dits «chauds», actifs à une température comprise entre 37 et 40°C. Elles sont les plus fréquentes (environ 70 % des cas) ;
- les AHMI à auto-anticorps dits «froids», actifs à des températures inférieures à 30°C. La «maladie chronique des agglutinines froides» (MAF) est la forme la plus fréquente d’AHMI à auto-anticorps « froids ».
-
Les causes d’AHMI:
Le système immunitaire, dont la fonction essentielle est normalement d’assurer la défense de l’organisme vis-à-vis des agressions extérieures (bactéries, virus…), dysfonctionne et produit de façon anormale des anticorps dirigés contre les hématies.
Les causes exactes de l’AHMI sont souvent inconnues.
Néanmoins, certains facteurs déclenchants peuvent parfois être identifiés :
-
-
- une infection virale
- la prise de certains médicaments (alpha-méthyl-dopa..)
- l’association à une autre maladie auto-immune (un lupus par exemple) ou encore à la multiplication anormale de cellules des ganglions lymphatiques appelée lymphome.
-
L’anémie hémolytique à médiation immune n’est pas contagieuse.
Certaines sont héréditaires :
-
-
- Anomalie de l’hème et de l’hémoglobine
- Anomalies de la membrane des hématies (Schnauzer Nain, Somali, Abyssin)
- Déficit enzymatique :
- Déficience en pyruvate kinase (Basenji, West Highland white terrier)
- Déficience en phosphofructokinase (Épagneuls anglais, Cockers*)
- Anémie hémolytique non sphérocytaire (Caniche, Beagle)
-
Les signes d’AHMI :
Cette maladie provoque deux grands types de manifestations :
-
-
- des manifestations liées à la baisse de la quantité de globules rouges dans le sang (anémie) : un essoufflement pour des efforts peu importants, une pâleur des muqueuses, une fatigue générale.
- des manifestations liées à la destruction accrue des globules rouges (hémolyse) avec une coloration jaunâtre de la peau et/ou des conjonctives (blanc de l’œil), appelée ictère ou jaunisse, et des urines qui peuvent parfois être très foncées (rouge/brun). Vomissements, diarrhées, parfois augmentation du volume des boissons et des urines.
-
Les anticorps anormaux (auto-anticorps) provoquent la destruction des globules rouges, l’hémolyse.
L’hémoglobine, qui est une protéine contenue dans les globules rouges et qui distribue l’oxygène à tout l’organisme, se retrouve alors détruite. C’est cette destruction qui explique à la fois l’anémie (sans hémoglobine, le sang né peut plus transporter l’oxygène, ce qui provoque les manifestations décrites plus haut) mais aussi la jaunisse (ictère) et la coloration foncée des urines. En effet, l’hémoglobine est rapidement transformée en bilirubine, qui est un pigment brun-jaune. C’est cette bilirubine libre qui,en s’accumulant dans le sang, va colorer la peau et les yeux et être responsable de la jaunisse.
L’hémolyse épuise les reins et l’animal développe une insuffisance rénale; des toxiques dangereux s’accumulent.
Parfois, s’associe une destruction des plaquettes sanguines (thrombocytopénie) qui peut se traduire par des saignements au niveau des muqueuses.
Le diagnostic d’AHMI:
La prise de sang met en évidence :
-
-
- l’anémie : baisse du taux d’hémoglobine dans le sang
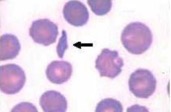
- l’hémolyse : destruction des globules rouges (augmentation de l’haptoglobine, du LDH… présence de schizocytes : résidus de globules rouges détruits) et présence de nombreux réticulocytes : la moelle osseuse fonctionne normalement et produit un maximum de nouveaux globules rouges)
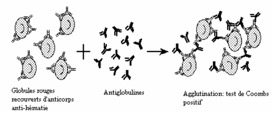
- test de Coombs direct positif : mise en évidence d’auto-anticorps dirigés contre les propres globules rouges
-
Le traitement de l’AHMI:
Dans le cas des AHMI à auto-anticorps «chauds» ce traitement est quasiment toujours nécessaire. Celui-ci repose avant tout sur des médicaments, les corticoïdes (cortisone ou ses dérivés). En moyenne, 80% des malades répondent favorablement au traitement par corticoïdes. Sinon, d’autres traitements (immunosuppresseurs) peuvent être indiqués selon les cas.
Des transfusions sanguines peuvent également être nécessaires pour «passer un cap» au début, lorsque l’anémie est importante et mal tolérée, en attendant l’efficacité du traitement médicamenteux.
Dans tous les types d’AHMI, la prise régulière de «folates» (vitamine B9) est utile pour faciliter la fabrication plus rapide des globules rouges par la moelle osseuse.
Si l’AHMI est liée à une cause, le traitement de la cause est évidemment primordial.
Selon les études, les taux de survie des chiens sont extrêmement variables (mortalité de 30% à 100% selon les centres). On note néanmoins deux profils de survie :
-
-
- certains chiens décèdent en un mois
- les chiens qui survivent au-delà du deuxième mois ont une durée moyenne de survie de presque trois ans.
-
La splénectomie est parfois recommandée. Il s’agit d’une intervention chirurgicale lourde (ablation de la rate) et dangereuse, impliquant une hospitalisation et des douleurs, dont le retentissement est loin d’être négligeable.
Le pronostic des chiens est plus favorable s’ils sont jeunes.
Bibliographie:
- Les anémies et les thrombopénies auto-immunes chez les carnivores domestiques – Thèse pour le doctorat vétérinaire, E. Donzel, Faculté de Médecine de Créteil,2007
- L’anémie hémolytique auto-immune, Encyclopédie Orphanet Grand Public, Août 2009-www.orpha.net/data/patho/Pub/fr/AnemieHemolytiqueAutoImmune-FRfrPub13392.pdf
- Garden OA (2010). Immune-mediated diseases and therapies, Textbook of Veterinary Internal Medicine, Seventh edition (Ettinger SJ et Feldman EC), Saunders-Elsevier, St. Louis,729–43.
- Helmond SE et al (2010). Treatment of immune-mediated hemolytic anemia with individually adjusted heparin dosing in dogs, J Vet Intern Med 24 :597–605.
- Anémie hémolytique à médiation immunitaire (AHMI) chez le chien ou le chat - http://www.vet24.fr/anemie-hemolytique-auto-immune-chien-chat_245.aspx?me=265
- Miller E (2009) Immune-mediated haemolytic anemia. Kirk’s Current Veterinary Therapy XIV — editors JD Bonagura & DC Twedt, Saunders Elsevier, St Louis pp 266
- Threlfall AJ et coll: Analysis of DLA-DQB1 and polymorphisms in CTLA4 in Cocker spaniels affected with immune-mediated haemolytic anaemia. Canine Genetics and Epidemiology2015, 2:8 doi:10.1186/s40575-
